
[e경제뉴스 박문 기자] 보건복지부와 식품의약품안전처는 27일부터 내년 1월 16일까지 '의료기기산업 육성 및 혁신의료기기 지원법 시행령 및 시행규칙' 제정안을 입법예고한다고 밝혔다.
혁신형 의료기기기업 인증 기준과 혁신의료기기군 지정 절차 등이 포함된 이 법은 내년 5월부터 시행된다.
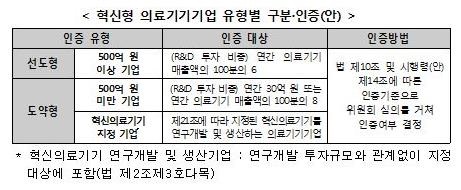
인증 대상은 일정규모 이상 연구개발(R&D) 투자 기업으로 연간 의료기기 매출액 500억원을 기준으로 한다. 매출 상위기업은 선도형, 미만은 도약형으로 나눈다.
시행령은 이같이 혁신형 의료기기업의 인증기준을 구체화했다.
인증대상을 연간 의료기기 매출액 500억 원을 기준으로 일정규모 이상 연구개발(R&D) 투자 기업을 혁신형 의료기기기업으로 했다.
인증기준은 혁신형 의료기기기업의 인증 심의를 위한 세부 인증기준과 인증의 지위 승계심의 예외요건, 인증의 취소, 우대조치 중단 및 반환 절차, 기업 유형구분 등으로 정했다.
종합지원센터 신청과 산업육성위원회 평가를 거쳐 복지부 인증을 받은 기업은 국가연구개발사업 등 정부 지원사업과 복지부 장관 소관 지원 사업 우선 참여 기회가 주어진다.
혁신의료기기군은 기술집약도가 높고 혁신속도가 빠른 첨단기술, 획기적인 개선이 예상되는 분야, 핵심기술 개발이 시급한 분야, 희귀·난치성 질환 치료 등에 필요하지만 국내 수급이 어려운 분야 등이 해당한다.
복지부가 핵심 기술의 보편화 여부와 유효기간(3년) 이내에 상용화 가능성을 종합적으로 고려해 고시하면 식약처와의 공동 검토 등을 거쳐 지정된다.
혁신형 의료기기 지원을 위한 인·허가 특례 규정도 총리령으로 제정한다.
혁신의료기기로 지정받은 의료기기는 허가·인증 신청 시 우선 심사를 요청할 수 있다.
혁신의료기기소프트웨어는 제조기업 인증제도를 통해 사용목적 변경 등 식약처장이 고시하는 중대 변경사항의 경우에만 변경 허가·인증을 받도록 하고 나머지 변경사항은 보고로 대체할 수 있도록 규정했다.
복지부와 식약처는 "내년 5월 시행에 차질이 없도록 이번 시행령 및 시행규칙 제정을 추진하고 이후 세부 고시 등을 통해 구체적인 제도 운영방식 등을 마련해 나갈 것"이라고 했다.
